新的研究表明细菌也会饥饿
你有没有饿得生气,也就是所谓的“饿肚子”?微生物学和免疫学系助理教授Adam Rosenthal博士的新研究发现,一些细菌细胞也会变得愤怒,将有害毒素释放到我们的体内,使我们生病。
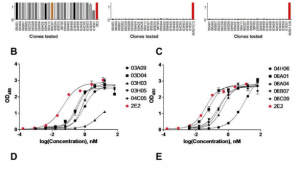
罗森塔尔和他来自哈佛大学,普林斯顿大学和丹尼斯科动物营养学的同事使用最近开发的一项技术发现,细菌群落中基因相同的细胞具有不同的功能,一些成员表现得更温顺,而另一些成员则产生使我们感到不适的毒素。
“细菌的行为与我们传统上认为的要大不相同,”罗森塔尔说。“即使我们研究一个基因相同的细菌群落,它们的行为方式也不相同。我们想知道原因。
发表在《自然微生物学》上的研究结果对于理解细菌群落如何以及为什么将职责推迟到某些细胞尤为重要,并可能导致进一步解决抗生素耐受性的新方法。
罗森塔尔决定仔细研究为什么有些细胞充当“乖巧的公民”,而另一些细胞则充当“坏人”,负责将毒素释放到环境中。他选择了产气荚膜梭菌(一种杆状细菌,可以在人类和其他脊椎动物、昆虫和土壤的肠道中找到)作为他的研究微生物。
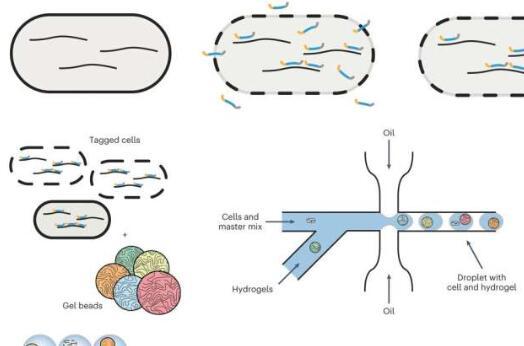
在一种称为微流体液滴发生器的装置的帮助下,他们能够将单个细菌细胞分离或分割成液滴以解码每个细胞。
他们发现不产生毒素的产气荚膜梭菌细胞营养充足。另一方面,产毒素的产气荚膜梭菌细胞似乎缺乏这些关键的营养素。
“如果我们提供更多的这些营养物质,”罗森塔尔假设,“也许我们可以让产生毒素的细胞表现得更好一点。
然后,研究人员将不良行为者细胞暴露于一种叫做醋酸的物质中。他们的假设听起来是正确的。不仅整个社区的毒素水平下降,而且不良行为者的数量也减少了。但在如此惊人的结果之后,更多的问题正在出现。
既然他们知道营养物质在毒性中起着重要作用,罗森塔尔想知道环境中是否发现了可能“开启”其他类型的感染中毒素产生的特定因素,或者这一新发现是否仅适用于产气荚膜梭菌。
也许最重要的是,罗森塔尔认为,将营养物质引入细菌可以为动物和人类提供一种新的替代疗法。
例如,模式生物产气荚膜梭菌是鸡舍中强大的敌人。随着食品工业不再使用抗生素,家禽对迅速传播的致命疾病毫无防备。Rosenthal等人最近的发现可能为农民提供了一种不使用抗生素即可减少致病菌的新工具。
至于我们人类,还有更多的工作要做。罗森塔尔正在与UNC的同事合作,将他最近的发现应用于解决抗生素耐受性问题。当一些细菌能够躲避药物靶标时,即使社区没有进化出突变以使所有细胞对抗生素产生抗药性,也会发生抗生素耐受性。这种耐受性可能导致治疗效果降低,但控制耐受性的机制尚不清楚。
与此同时,罗森塔尔将继续研究这些日益复杂的细菌群落,以更好地了解它们为什么这样做。
免责声明:本文为转载,非本网原创内容,不代表本网观点。其原创性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容、文字的真实性、完整性、及时性本站不作任何保证或承诺,请读者仅作参考,并请自行核实相关内容。